| Hartchrom | ||
|
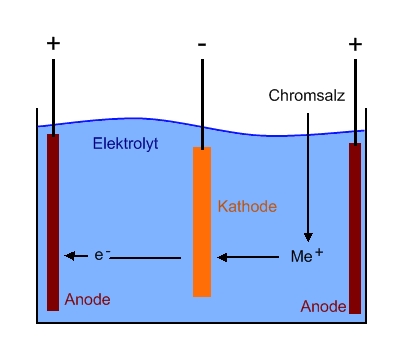
Die Abscheidung von Hartchrom in der galvanischen Zelle Unter „galvanisieren“ versteht man im Allgemeinen die elektrochemische Abscheidung von Metallen auf der Bauteiloberfläche durch das Anlegen einer äußeren Gleichstromquelle. Hierbei wird das zu beschichtende Bauteil als Kathode(-) geschaltet, an der im Beschichtungsprozess die positiv geladenen Metallionen als metallische Schicht (hier Hartchrom) abgeschieden werden. Die Anoden(+) bestehen meist aus dem Beschichtungsmaterial und gehen während der Elektrolyse in Lösung und stellen so die Metallionen zur Abscheidung zur Verfügung. Zur Veranschaulichung des Prinzips der galvanischen Zelle dient die folgende Skizze:
Je nach gefordertem Beschichtungsmaterial werden verschiedene Elektrolyte eingesetzt. Die gängigen Beschichtungen sind Kupfer, Nickel, Chrom, Hartchrom, Zink, chem. Nickel, usw. Die Hartchrom - Schicht wird aus einem Chromschwefelsäure-Elektrolyten, so wie oben dargestellt, abgeschieden. Die wichtigsten Eckdaten zur Abscheidung von Hartchrom sind in der obigen Abbildung enthalten. Die Beschichtung mit Hartchrom stellt in vielerlei Hinsicht eine Besonderheit unter den elektrolytischen Abscheidungsverfahren dar. Als ein großes Manko ist der geringe Wirkungsgrad der Hartchrom - Abscheidung zu nennen. Beim Beschichten mit Hartchrom kommt es zu einer Vielzahl von elektrochemischen Reaktionen, hier ist vor allem die Bildung von Wasserstoff zu nennen, die es in der handwerklichen Praxis nicht erlauben, einen Wirkungsgrad von 30% zu erreichen. Es gehen bei der Abscheidung von Hartchrom also selbst bei einem absolut neuen Elektrolyten bereits über 70% der eingebrachten Energie für diverse Nebenreaktionen verloren. Eine weitere Besonderheit der Hartchrom - Abscheidung ist es, dass anders als z.B. beim galvanischen Vernickeln, Verkupfern oder Verzinken, wo die eingesetzte Anode aus dem jeweiligen Beschichtungsmaterial besteht und als Metallquelle zur Abscheidung dient, beim Beschichten mit Hartchrom Anoden aus Blei oder platiniertem Titan eingesetzt werden. Das Metall zur Abscheidung der Hartchrom - Schicht muss dem Prozess (genauer dem Elektrolyt) also extra zugeführt werden. Dies geschieht in Form von „Chromsalz“ (CrO3). Die Menge an abgeschiedenem Hartchrom entspricht also direkt der hinzu dosierten Menge an CrO3. Betrachtung der Hartchrom - Abscheidung Die Menge an abgeschiedenem Hartchrom lässt sich sehr einfach stöchiometrisch berechnen: Atommassen: Cr 52 O 16 Masse CrO3: 52 + 16x3 = 100 . . . . . . . . . . . . . . . . . |